La metilación fluctuante abre una nueva era para entender y predecir la evolución del cáncer
Índice
La evolución tumoral es un proceso dinámico: los tumores crecen, generan clones, adquieren ventajas selectivas y, en algunos casos, desarrollan resistencia terapéutica. Aunque este proceso explica gran parte del comportamiento clínico del cáncer, su reconstrucción directa ha sido tradicionalmente compleja, requiriendo seguimientos longitudinales prolongados, múltiples biopsias o tecnologías avanzadas como la secuenciación de célula única.
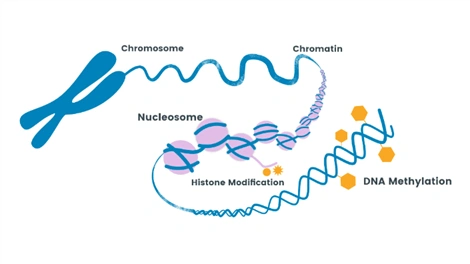
Un estudio reciente publicado en Nature y con una destacada participación de investigadores de diversos centros españoles, describe una aproximación innovadora basada en la metilación fluctuante del ADN, demostrando que determinados sitios CpG (fCpGs) presentan variaciones aleatorias a lo largo del tiempo que no alteran la función génica, pero dejan una huella estable heredable por las células hijas.
Este patrón actúa como un auténtico registro epigenético de la historia evolutiva del tumor, permitiendo identificar clones, subclones y eventos de expansión clonal a partir de una única muestra.1
Estas fluctuaciones no alteran la función del gen, pero dejan una huella estable en las células, de manera que aquellas que compartan un ancestro común poseerán un patrón de metilación casi idéntico, como si cada clon tumoral llevara su propia firma epigenética. En la práctica, esto convierte a la metilación fluctuante en un “código de barras evolutivo” capaz de registrar los eventos históricos del tumor.
Se trata de una metodología computacional que transforma perfiles de metilación en bulk, obtenidos mediante arrays de metilación o secuenciación masiva (NGS), en modelos capaces de reconstruir la evolución tumoral con alta resolución temporal. De forma destacada, EVOFLUx no requiere nuevas tecnologías experimentales, sino que aprovecha datos generados con plataformas ampliamente implantadas en los laboratorios de diagnóstico e investigación molecular.
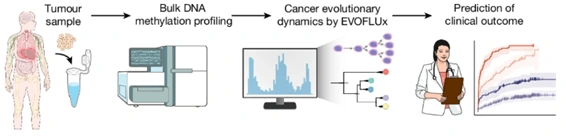 Imagen obtenida del artículo original.
Imagen obtenida del artículo original.
Aplicado a casi 2.000 muestras de neoplasias linfoides, el modelo permitió estimar parámetros clave como la velocidad de crecimiento tumoral, la edad real del tumor desde su origen, el tamaño efectivo de la población clonal y las tasas de epimutación. Estos análisis revelaron que cada tipo y subtipo de cáncer presenta una firma evolutiva característica, con claras diferencias entre tumores pediátricos de crecimiento rápido y neoplasias crónicas del adulto, más antiguas y heterogéneas. Además, EVOFLUx identificó subclones seleccionados, efectos de mutaciones relevantes como TP53 y, de forma notable, casos con tumores de origen independiente coexistiendo en un mismo paciente.
De forma sorprendente, EVOFLUx incluso identificó pacientes con dos tumores independientes coexistiendo, algo extremadamente difícil de detectar con herramientas clásicas.
«Uno de los descubrimientos más impactantes fue que, en pacientes con CLL que desarrollaron transformación de Richter, la célula precursora había divergido más de 30 años antes del diagnóstico clínico. Es decir, la agresividad del tumor podía estar “programada” décadas antes de manifestarse, lo que cambia por completo la forma de entender el riesgo clínico evolutivo.»
La validez biológica y clínica de esta aproximación se confirmó mediante comparaciones con WES, WGS y series longitudinales de más de 15 años, demostrando que la metilación bulk analizada mediante NGS puede reflejar la evolución tumoral con una sensibilidad comparable (e incluso superior en algunos contextos) a la secuenciación genómica convencional.
En conjunto, EVOFLUx introduce la historia evolutiva del tumor como una nueva variable clínica medible, integrable en flujos de trabajo basados en NGS. Esta aproximación amplía el valor del análisis de metilación, posicionándolo como una herramienta estratégica en oncología de precisión, con potencial aplicación transversal en distintos tipos de cáncer y en muestras de biopsia líquida.
¿Quieres saber más?
Puedes consultar el artículo completo en el siguiente enlace:
Fluctuating DNA methylation tracks cancer evolution at clinical scale | Nature
Y si estás interesado en cómo podemos ayudarte a implementar en tu rutina los estudios de metilación y el diagnóstico molecular mediante NGS contáctanos en info@dlongwood.com o navega a través de nuestro sitio web.
Contactar con el equipoReferencias
1. Gabbutt, C. et al. Fluctuating methylation clocks for cell lineage tracing at high temporal resolution in human tissues. Nat. Biotechnol. 40, 720–730 (2022).
2. Gabbutt, C. et al. Fluctuating DNA methylation tracks cancer evolution at clinical scale. Nature 645, 764–773 (2025).

