La multiómica espacial revela el impacto del Alzheimer a nivel subcelular
Índice
El análisis espacial de alta multiplexación ha revolucionado nuestra comprensión de los tejidos, pero cuando nos adentramos en el cerebro humano, nos topamos con un muro: la complejidad morfológica de las neuronas. Históricamente, la mayoría de los flujos de trabajo en ómica espacial se han centrado en el soma (el cuerpo celular). ¿El problema? Esta aproximación deja en un «punto ciego» procesos biológicos cruciales que ocurren en las intrincadas proyecciones neuronales, como la traducción localizada de ARN o el posicionamiento de orgánulos fundamentales.
En enfermedades neurodegenerativas como el Alzheimer (AD), la disfunción no empieza en el núcleo, sino que a menudo se manifiesta en el enriquecimiento mitocondrial en las sinapsis. Para capturar esta realidad, necesitamos una resolución que vaya más allá de los métodos tradicionales.
El fin del «punto ciego»: Segmentación guiada por proteínas
En el reciente AGBT 2026, Bruker presentó un póster que marca un antes y un después en este desafío metodológico: «Mapping organelle-associated mRNA localization in Alzheimer’s disease brain via spatial multiomics».
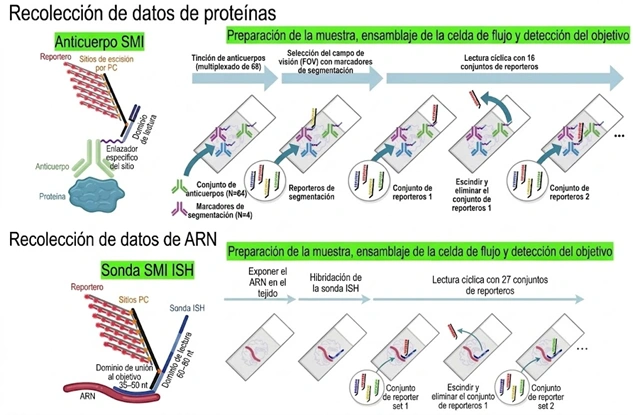
Utilizando el CosMx® Spatial Molecular Imager (SMI), el equipo de Bruker ha logrado una detección simultánea de proteínas de alto multiplexado (64-plex) y ARN (panel de 6K o genoma completo WTX) en la exacta misma sección de tejido cerebral humano.
¿El verdadero avance? Usar los datos morfológicos de las proteínas para redefinir la segmentación celular. Al abandonar la «vieja» segmentación basada únicamente en morfología de ARN y utilizar el panel de proteínas como mapa estructural, el algoritmo logra asignar los transcritos a las células con una precisión sin precedentes, capturando dendritas, axones y microglía que antes quedaban fuera del radar.

Hallazgos clave en tejido con Alzheimer
La aplicación de este framework multiómico en matrices de tejido sano y con Alzheimer parietal, occipital y cerebeloso ha arrojado datos reveladores:
Una herramienta, múltiples aplicaciones
Aunque este estudio se centra en el Alzheimer, la capacidad del CosMx® SMI para perfilar la biología espacial mitocondrial tiene implicaciones masivas para otras áreas, incluida la oncología, donde la transferencia de mitocondrias de neuronas a células cancerosas juega un papel vital en el metabolismo tumoral.

Si quieres saber más sobre esta tecnología, entre en la ficha del producto a aquí.
Si tu investigación exige no perder de vista ni un solo transcrito en tejidos de alta complejidad morfológica, este trabajo es de lectura obligatoria.

